氷・水・水蒸気…
水の三態
私たちは日常の中で、水を冷やせば氷になり、
氷に熱を加えると水に戻り、
さらに熱を加えていけば水蒸気になることを
当たり前のように体験しています。
しかし、水は人為的な作用を加えずに、
自然条件の中でも固体、液体、気体と
姿を変えることができます。
私たちにとって、水ほど
当たり前のものもありませんが、
実は水ほど不思議な物質もありません。
水のもつ能力や謎には、
いまだ解明できていない部分があります。
水分子の構造
水の分子は、化学記号からわかるとおり水素原子(H)2つと酸素原子(O)1つが結合してできていますが、この水分子1つでは液体になりません。水という液体になるためには、水分子がたくさん連なることが必要です。物質を構成する分子と分子がつながるための力にはいろいろな種類がありますが、水分子の場合は酸素側がマイナスの電荷、水素側がプラスの電荷を持つようになり、いわば磁石のような働きを持っているために、正負で引き合う電気的な力によって結合します(水素結合)。この水素結合により、水分子間がつながり、水分子の集合(水クラスター)が形成されます。常温の水では、5~6個から十数個の分子がクラスタを形成しています。
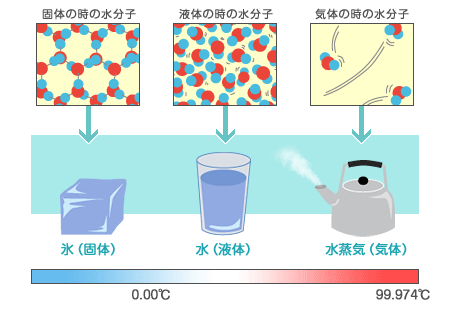
水の三態・液体=水
水が液体の状態であるのは、1気圧のもとでは、その温度が0.00℃~99.974℃までの間です。
(元々、水の沸点は沸点を100℃と決めたが、「1℃」の定義が見直されたため、水の沸点は現在厳密には99.974度に定義されている。)
水分子は、いくつかが集まり、集団で1つの固まりになったり、それがまた崩れたりしながら、でたらめな方向に向かって自由に運動しています。水が様々な形に変化できるのは、分子がこのように自由に動いているためです。外から熱を加えていくと、この運動が激しくなり、水分子は集合した固まりでいられなくなってきます。
水の三態・気体=水蒸気
水は99.974℃(1気圧下)に達すると沸騰し、分子の集団はバラバラになります。
水分子は激しく動き、猛烈なスピードで空間を飛び回ることになります。
水蒸気という気体は目に見えません。沸いたやかんの口から出る白い湯気は、水蒸気が周囲の空気で冷やされて水の粒に戻った状態のもの。やかんの口から出る透明な気体が水蒸気で、白い湯気の部分は液体です。
水の三態・固体=氷
水が0.00℃以下(1気圧下)になると、運動するための熱エネルギーが極端に低く、水分子は動きをとめて互いに結合します。水分子は、曲がった形をしているために、分子同士はすきまが多い形でしか結合できません。
そのために、分子と分子の間にすきまができて距離があき、その分体積が増えることになります。水を凍らせるとかさが増えるのは、そのためなのです(増える量は、約10パーセント)。普通の液体は固体になると密度があがり、体積は小さくなります。固体になると体積が増えるのは、他の多くの物質とは異なる水の性質です。
水の不思議・自然現象編
自然現象の中に見ることのできる、水の特異な性質を考えてみましょう。
1)岩石の風化・霜柱→「氷になると体積が増える」
冬の風物詩・霜柱は、ごく簡単に言えば地中の水分が凍って体積が増え、地表の土をおしのけて出たもの。また岩石の風化にも水は大きく関わっています。たとえば、岩石の亀裂にしみこんでいた水が凍結し、体積を増し、その力で亀裂を押し広げます。そしてこれを繰り返すうちについに岩石が割れるのです。
2)氷山が沈まず海に浮いている→「氷になると密度が下がる」
凍ると体積が増えるということは、同じ体積で比較した場合、氷のほうが水よりも軽いということになります。飲みものに入れた氷が浮かぶのも、氷山が海の上に浮かんでいるのもそのためです。

3)湖や池の水は、表面から凍り始める→「水は3.98℃のときに一番重い」
水の密度は、
(1) 氷(0度):0.91671グラム/立方センチメートル
(2) 水(0度):0.999840グラム/立方センチメートル
(3) 水(3.98度):0.999973グラム/立方センチメートル
となっています。その後温度が上がるにしたがって密度は少しずつ小さくなり、1気圧下の沸点である99.974度で0.95835グラム/立方センチメートル程度になります。
冬、気温が零度を下回ると、湖や池の水も冷え始めます。温度が3.98℃にむかって下がっているとき、水はどんどん重くなり、下の方へ移動します。3.98℃から更に冷えると今度は軽くなり、上にとどまります。そしてそのまま水面から凍結し始めるのです。湖や池が凍りついても、中で魚が生きていけるのは水のこうした性質によります。
4)真夏でも海や川がお湯にならないでいられる→「水の比熱が大きいから」
比熱というのは物質1グラムの温度を1℃上げるのに必要な熱量のことです。「水の比熱が大きい」というのは、水を熱くするためにはたくさんの熱量が必要ということで、つまり「水は温まりにくく、冷めにくい」物質です。
(ちなみに、水の比熱を1とすると油はその半分、つまり同量の水と油を1度温めるのに水は2倍の熱を必要とします。)
もし水の比熱が小さかったら、海や川はたちまち温度が上がり、多くの生物にとっては生きていけない環境になってしまうでしょう。地球が生物にとって生きていける環境を保っているのは、水が熱を蓄積し、気温の変動をゆるやかにしているおかげなのです。
水の不思議・暮らし編
つぎに、暮らしの中で見ることのできる水の特徴について考察します。
1)スケートが楽しめる→圧力をかけると、氷が溶ける
スケート靴をはくと、なぜあんなに滑りやすくなるのでしょうか。それは、スケート靴の刃と氷のあいだに水があり、その水が潤滑剤の役割をしているからです。氷は溶けるものなので、水があるのは当然だと感じるかもしれませんが、氷が自然に、気温が高いために溶けて水になっているのであれば、スケートリンク中が水びたしになるはずです。スケートリンクの表面の氷は、人間のはいたスケート靴の刃が上に乗ったときには水になりますが、人間が通過してしまうとふたたび氷に戻ります。これも水の特質の一つです。
(なお、最近の研究ではその他の要因もわかってきています。)
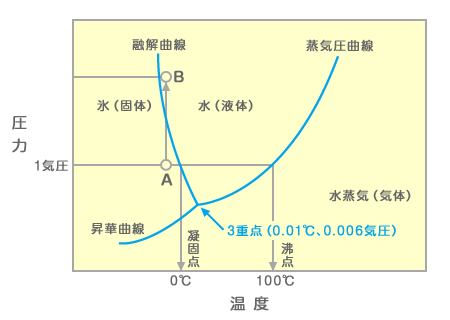
物質の状態(固体、液体、気体)は圧力と温度によって決まります。1気圧のもとでは、水は0.00度以下になると固体になり、99.974℃になると気体になります。気圧を上げると、水は99.974℃でも沸騰しなくなりますが、逆に圧力を下げると、99.974℃未満でも沸騰してしまいます。このように、蒸気圧曲線が右上がりになるのは全ての液体に共通する性質なのです。ところが、氷の融点の曲線を見ると、圧力を上げると融点は下がります。つまり、圧力をかけると氷は0.00度未満でも溶け始めるのです。このように融解曲線が左上がりなのは水だけの特徴です(水は固体になると密度がさがる。圧力がかかるとできるだけ体積を小さくしようとし、水になったほうが密度があがり体積が小さくなれるため、溶けて水になる)。
人間の重さがスケート靴の刃を通して圧力として氷にかかると、その部分の氷は溶けてしまいます。人間が通り過ぎて圧力がもとに戻ると、水は1気圧の条件下にもどるため、氷に戻ります。靴の刃とリンクのあいだには常に潤滑剤として水が存在するが、リンク中が水浸しにならないのはこのような水の性質のためなのです。
2)タオルで体がふける→毛細管現象
タオルやガーゼの一部を水につけると、そこから水が吸収されてタオルやガーゼは濡れていきます。これは毛細管現象によるものです。
タオルやガーゼは、細い糸がよりあわされ織られてできているため、縦糸と横糸、繊維同士のあいだにもたくさんの小さなすきまがあります。そこに水が侵入していくのです。毛細管現象というのは、液体が細い管や微小なすき間に浸透していくこと。この「すきまに浸透していく力」というのは、管の径が小さいほど、また液体の表面張力が大きいほど強くなります。
水の表面張力は並はずれて大きいのです。
液体の温度20℃での表面張力の一覧を見ると、エタノールが22.3ダイン/cm(※1)、酢酸が27.6ダイン/cmであるのに対し、水は72.75ダイン/cmもあります。これは、水分子の結合力が強く、分子どうしで引っぱる力が強いためです。また、タオルやガーゼなどの天然繊維は親水基(※2)を多く持っているので、よけい水になじみやすく、水の侵入速度はより速くなります。風呂あがりにぬれた体や髪をタオルで乾かすことができるのは、この水の性質のおかげといえます。
- ダイン(dyn)とは、力のCGS単位。「1ダインは、質量1グラムの物体に働くとき、その方向に1cm/s2の加速度を与える力と定義されている。」(岩波理化学辞典5版)
- 分子がその一部に持つ、水分子となじみやすい構造。たとえば水素結合しやすい構造をもっていたり、電気的に結合しやすい性質を持っていたりする。
参考文献
- 播磨裕・岡野正義・山崎岳 他/共著 『水の総合科学』 三共出版
- 平澤猛男/著 『水は永遠の友』 研成社
- 石原信次/著 『知っておきたい水のすべて』 インデックス・コミュニケーションズ
- 上平恒/著 『水とはなにか』 講談社
- 左巻健男/著 『水と空気の100不思議』 東京書籍
- 稲場秀明/著 『氷はなぜ水に浮かぶのか』 丸善
- 中川鶴太郎/文 村田道紀/絵 『氷・水・水じょう気』 岩波書店
- ウォルター・ウィック/著 『ひとしずくの水』 あすなろ書房
- 『学研の観察・実験シリーズ 空気中の水の変化』 学習研究社
- 高橋裕 他/編 『水の百科事典』 丸善 1997
- 長倉三郎 他/編 『岩波理化学辞典5版』 岩波書店
くらしと水
私たちの毎日に欠かせない水。
今日から役立つ、くらしの水知識をご紹介します。
世界の水文化
地域の気候や状況によって、人々と水との付き合いは様々。世界各地の特徴的な水の活用をご紹介します。
水の科学
ひと言で「水」と言っても、実は色々な側面が。水の性質や種類、生命と水との関係を解き明かします。